2026年3月24日,北京大学-云南白药国际医学研究中心主任詹启敏院士团队在国际权威期刊 《Advanced Science》上在线发表研究论文“Halofuginone is a Molecular Glue Degrader of Integrin β4”。该研究揭示了天然产物Halofuginone(常山酮)作为一种全新的分子胶药物,能够高效降解与多种实体肿瘤恶性进展密切相关的跨膜蛋白整合素β4,为食管鳞状细胞癌(ESCC)等多种高表达整合素β4的肿瘤带来了全新的潜在治疗方案。研究已证实,通过化学修饰优化后的PEG化常山酮保留了抗肿瘤活性,同时显著降低了系统毒性。
核心发现
1. 新型分子胶降解剂的发现:
研究团队通过高通量筛选天然产物化合物库,发现天然产物常山酮能够有效抑制多种食管鳞癌细胞系的生长与侵袭。
2. 精确作用靶点揭示:
借助药物亲和性响应靶点稳定性(DARTS)及表面等离子共振(SPR)等生物物理技术,研究证实常山酮直接结合并诱导整合素β4的降解。整合素β4是一种在许多实体瘤中高表达且与临床不良预后相关的跨膜蛋白。
3. 独特的降解机制:
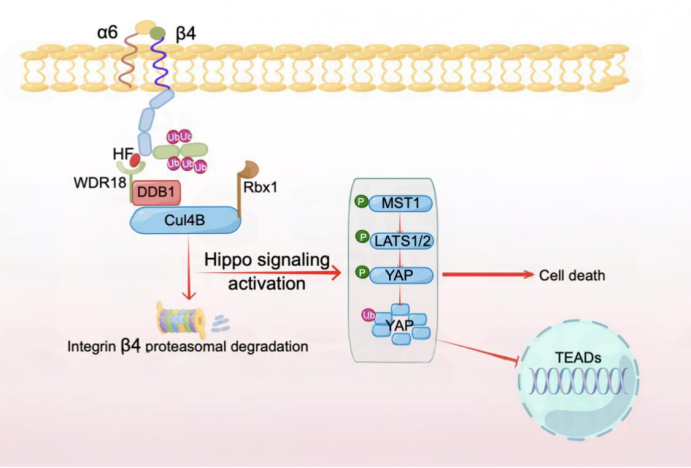
该研究首次阐明常山酮作为一种分子胶发挥作用,能将整合素β4招募至一种名为CRL4BWDR18的E3泛素连接酶复合体,从而通过泛素-蛋白酶体途径对其进行靶向降解。研究首次揭示了WDR18作为CRL4B复合物的一个新底物受体在分子胶降解过程中的关键作用。
4. 显著的抗肿瘤效果:
o 体外:常山酮处理能够剂量依赖性抑制食管鳞癌细胞的增殖、迁移、侵袭能力,并诱导细胞凋亡。
o体内:在患者来源异种移植(PDX)模型和肿瘤异种移植模型中,常山酮显著抑制了肿瘤生长。通过聚乙二醇(PEG)修饰得到的PEG-HF在保持抗肿瘤疗效的同时,有效减轻了模型小鼠的体重下降等副作用。
5. 作用机制深入研究:
研究表明,整合素β4的降解与下游Hippo信号通路的激活以及细胞凋亡相关。此外,常山酮与临床一线化疗药顺铂在抑制癌细胞活力上表现出良好的协同效应。
6. 临床相关性:
通过对食管鳞癌组织样本的分析,研究发现整合素β4在肿瘤组织中表达显著高于癌旁组织,且其高表达与患者淋巴结转移及更差的总生存期显著相关。这进一步确立了整合素β4作为一个有前景的抗癌治疗靶点。
研究背景与意义
整合素蛋白家族是细胞粘附和信号转导的关键介导者,与多种癌症的进展、转移和耐药性相关。尽管针对整合素αIIbβ3、α4β7等的药物已获批用于心血管和自身免疫性疾病,但针对整合素β4的有效靶向疗法仍然空白。靶向蛋白降解技术,特别是分子胶,为“不可成药”的靶点提供了革命性的策略。然而,分子胶的发现长期以来多依赖偶然性,且靶向跨膜蛋白的降解剂尤为稀缺。本项研究系统性地从天然产物库中发现了一种可靶向跨膜蛋白的分子胶,并通过机制解析,为后续通过基于结构的理性设计,筛选和优化更高效、更低毒的分子胶降解剂指明了方向。
研究团队
北京大学-云南白药国际医学研究中心詹启敏院士和北京大学肿瘤医院张维敏副研究员为共同通讯作者,北京大学-云南白药国际医学研究中心巩蔚助理研究员、北京大学肿瘤医院杨迪博士是本文的共同第一作者。该研究工作得到了国家重点研发计划、国家自然科学基金等多项基金的资助。
论文信息:
标题:Halofuginone is a Molecular Glue Degrader of Integrin β4
期刊:Advanced Science
日期:2026年
链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202515970